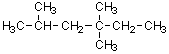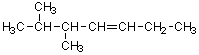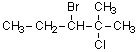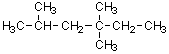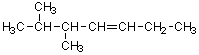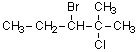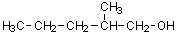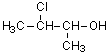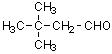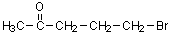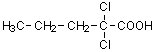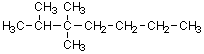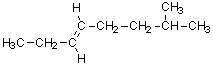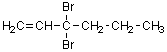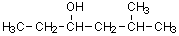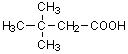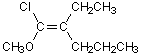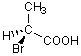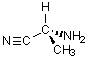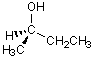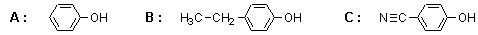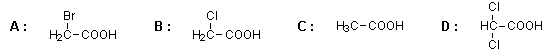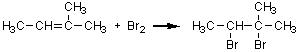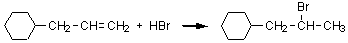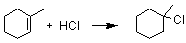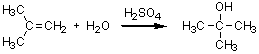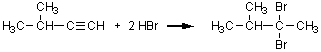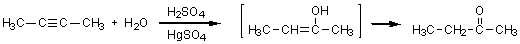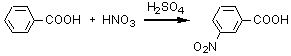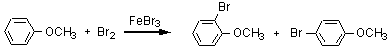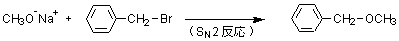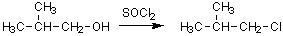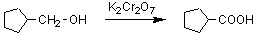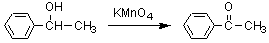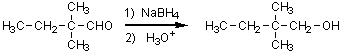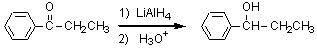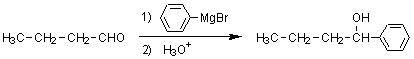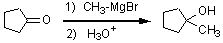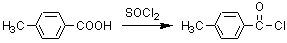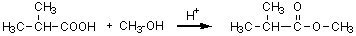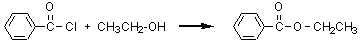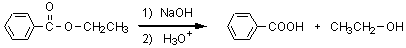基礎有機化学 演習問題 解答と解説 (平成25年度用)
1.次の化合物を命名せよ。ただし立体配置は考慮しなくてよい。
1)
|
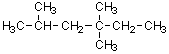 |
2)
|
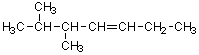 |
3)
|
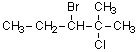 |
|
2,4,4-トリメチルヘキサン |
|
5,6-ジメチル-3-ヘプテン |
|
3-ブロモ-2-クロロ-2-メチルペンタン |
4)
|
 |
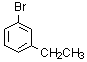
5)
|
 |
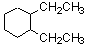
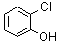
6)
|
 |
|
1,2-ジエチルシクロヘキサン
|
|
m-ブロモエチルベンゼン
|
|
o-クロロフェノール
|
7)
|
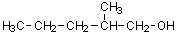 |
8)
|
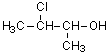 |
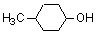
9)
|
 |
|
2-メチル-1-ペンタノール
|
|
3-クロロ-2-ブタノール
|
|
4-メチルシクロヘキサノール
|
10)
|
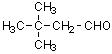 |
11)
|
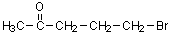 |
12)
|
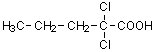 |
|
3,3-ジメチルブタナール
|
|
5-ブロモ-2-ペンタノン
|
|
2,2-ジクロロペンタン酸
|
2.次の化合物の構造式を書け。
1)
|
2,3,3-トリメチルヘプタン
|
2)
|
trans-7-メチル-3-オクテン
|
|
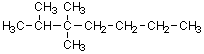 |
|
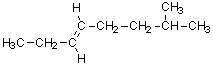 |
|
|
|
※演習問題中の「trans-2-メチル-5-オクテン」は誤りです。 |
3)
|
3,3-ジブロモ-1-ヘキセン
|
4)
|
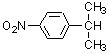
p-イソプロピルニトロベンゼン
|
5)
|
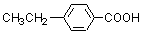
p-エチル安息香酸
|
|
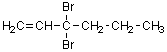 |
|
 |
|
 |
6)
|
5-メチル-3-ヘキサノール
|
7)
|
2,4-ジブロモペンタナール
|
|
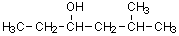 |
|
 |
| 8) |
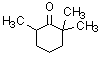
2,2,6-トリメチルシクロヘキサノン
|
9)
|
3,3-ジメチルブタン酸
|
|
 |
|
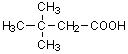 |
3.次の化合物の立体配置を E,Z で示せ。
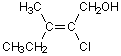
1)
|
 |
2)
|
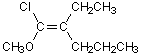 |
3)
|
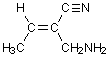 |
4)
|
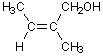 |
|
(Z)
|
|
(E)
|
|
(E)
|
|
(Z)
|
|
-CH2CH3 > -CH3
-Cl > -CH2OH
|
|
-Cl > -OCH3
-CH2CH2CH3 > -CH2CH3 |
|
-CH3 > -H
-C≡N > -CH2NH2 |
|
-CH3 > H
-CH2OH > -CH3 |
4.次の化合物の立体配置を R,S で示せ。
1)
|
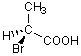 |
2)
|
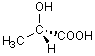 |
3)
|
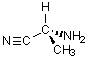 |
4)
|
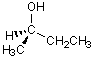 |
|
(S) |
|
(S) |
|
(R) |
|
(R) |
|
Br > COOH > CH3 > H
|
|
OH > COOH > CH3 > H |
|
NH2 > -C≡N > CH3 > H |
|
OH > CH2CH3 > CH3 > H |
5.次の化合物を酸性度の高いものから順に並べよ。
1)
|
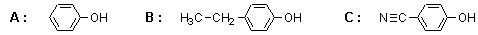 |
C > A > B
フェノールの酸性度は電子求引性基が結合していると高く、供与性基では低くなる。したがってこの中では求引性のシアノ基をもつ C の酸性度が最も高く、供与性のエチル基をもつ B が最も低くなる。
2)
|
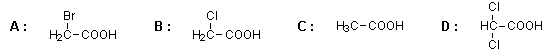 |
D > B > A > C
カルボン酸の酸性度も電子求引性基によって高くなるが、電気陰性度が高いほど、数が多いほどその効果は高まるので、Cl を二つもつ D の酸性度が最も高く、続いて Cl 一つの B 、Br 一つの A 、無置換の C の順になる。
6.次の反応の主生成物を書け。
1)
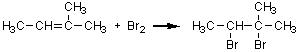 アルケンへのハロゲンの求電子付加。二重結合の一本が切断してそこに臭素が付加する。
アルケンへのハロゲンの求電子付加。二重結合の一本が切断してそこに臭素が付加する。
2)
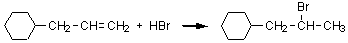 アルケンへのハロゲン化水素の求電子付加。ハロゲンと水素が二重結合の二つの炭素のどちらに結合するかはマルコウニコフ則に従う。
ハロゲンはより多くの置換基が結合している炭素に結合するので、この問題では右端の炭素(水素2個のみ)には H
が、右から2番目の炭素(アルキル基1個結合)には Br が結合する。
アルケンへのハロゲン化水素の求電子付加。ハロゲンと水素が二重結合の二つの炭素のどちらに結合するかはマルコウニコフ則に従う。
ハロゲンはより多くの置換基が結合している炭素に結合するので、この問題では右端の炭素(水素2個のみ)には H
が、右から2番目の炭素(アルキル基1個結合)には Br が結合する。
3)
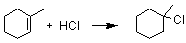 2)と同様にアルケンへのハロゲン化水素の求電子付加なので、同じくマルコウニコフ則に従う。二重
結合の二つの炭素のうち、下の炭素にはアルキル基が1個しか結合していないのに対し、上の炭素にはアルキル基が2個結合しているので、Cl
は上の炭素に、H は下の炭素に結合する。
2)と同様にアルケンへのハロゲン化水素の求電子付加なので、同じくマルコウニコフ則に従う。二重
結合の二つの炭素のうち、下の炭素にはアルキル基が1個しか結合していないのに対し、上の炭素にはアルキル基が2個結合しているので、Cl
は上の炭素に、H は下の炭素に結合する。
4)
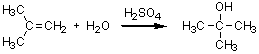 硫酸のような酸を触媒に用いるとアルケンに水が求電子付加する。水を HO-H と考え、ハロゲン化水素 X-H と同様にマルコウニコフ則に従うと考えればよい。したがって OH が左側の炭素に、H が右側の炭素に結合する。
硫酸のような酸を触媒に用いるとアルケンに水が求電子付加する。水を HO-H と考え、ハロゲン化水素 X-H と同様にマルコウニコフ則に従うと考えればよい。したがって OH が左側の炭素に、H が右側の炭素に結合する。
5)
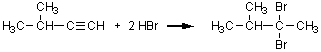 アルキンへはまず1分子の HBr
が求電子付加してアルケンとなり、さらにもう1分子が同様に付加するので、あわせて2分子のハロゲン化水素が付加できる。1段階目、2段階目ともにマルコ
ウニコフ則に従うので、結果として置換基の多い側の炭素に2つの Br が結合する。
アルキンへはまず1分子の HBr
が求電子付加してアルケンとなり、さらにもう1分子が同様に付加するので、あわせて2分子のハロゲン化水素が付加できる。1段階目、2段階目ともにマルコ
ウニコフ則に従うので、結果として置換基の多い側の炭素に2つの Br が結合する。
6)
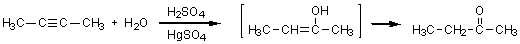 アルキンへの水の付加には硫酸に加えて硫酸水銀が触媒として必要である。まず1分子の水が付加すると、二重結合に直接 OH
が結合したエノール中間体が生成するが、これは2分子目の水が付加する前に、ケト-エノール互変異性により速やかに安定なケト体(ケトンやアルデヒド)に
異性化してしまうので、結果として水は1分子しか付加できず、生成物はアルコールでなくケトンとなる。
アルキンへの水の付加には硫酸に加えて硫酸水銀が触媒として必要である。まず1分子の水が付加すると、二重結合に直接 OH
が結合したエノール中間体が生成するが、これは2分子目の水が付加する前に、ケト-エノール互変異性により速やかに安定なケト体(ケトンやアルデヒド)に
異性化してしまうので、結果として水は1分子しか付加できず、生成物はアルコールでなくケトンとなる。
7)
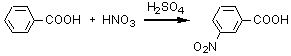 芳香族化合物の求電子置換反応。HNO3+H2SO4 はニトロ化の条件であるから、生成物にはニトロ基(-NO2)が導入される。導入位置は出発物質の置換基の配向性によって決まるが、-COOH はメタ配向性なので、メタ位にニトロ基が導入される。
芳香族化合物の求電子置換反応。HNO3+H2SO4 はニトロ化の条件であるから、生成物にはニトロ基(-NO2)が導入される。導入位置は出発物質の置換基の配向性によって決まるが、-COOH はメタ配向性なので、メタ位にニトロ基が導入される。
8)
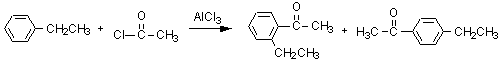 同じく求電子置換反応。ハロゲン化物+AlCl3
はフリーデル-クラフツ反応の条件なので、ハロゲン化物のアルキル基やアシル基がベンゼン環に導入される。今回はハロゲン化物が塩化アセチルであるから、
アセチル基が導入されることになる。出発物質のエチル基の配向性はオルト-パラ配向性なので、生成物はオルト置換体とパラ置換体の混合物となる。
同じく求電子置換反応。ハロゲン化物+AlCl3
はフリーデル-クラフツ反応の条件なので、ハロゲン化物のアルキル基やアシル基がベンゼン環に導入される。今回はハロゲン化物が塩化アセチルであるから、
アセチル基が導入されることになる。出発物質のエチル基の配向性はオルト-パラ配向性なので、生成物はオルト置換体とパラ置換体の混合物となる。
9)
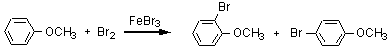 これも求電子置換反応。Br2+FeBr3 はブロモ化の条件であり、メトキシ基(-OCH3)はオルト-パラ配向性であるから、生成物はオルト位に Br が導入されたものとパラ位に Br が導入されたものの混合物となる。
これも求電子置換反応。Br2+FeBr3 はブロモ化の条件であり、メトキシ基(-OCH3)はオルト-パラ配向性であるから、生成物はオルト位に Br が導入されたものとパラ位に Br が導入されたものの混合物となる。
10)
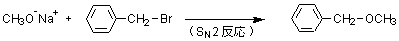 ハロゲン化アルキルの求核置換反応。SN2反応ではナトリウムメトキシドのメトキシドイオン(CH3O-)が求核試薬として Br の結合した炭素を攻撃し、O-C 結合が形成されると同時に Br- が脱離して、エーテルが生成する。これはウィリアムソン-エーテル合成と呼ばれ、SN2 反応の代表例。
ハロゲン化アルキルの求核置換反応。SN2反応ではナトリウムメトキシドのメトキシドイオン(CH3O-)が求核試薬として Br の結合した炭素を攻撃し、O-C 結合が形成されると同時に Br- が脱離して、エーテルが生成する。これはウィリアムソン-エーテル合成と呼ばれ、SN2 反応の代表例。
11)
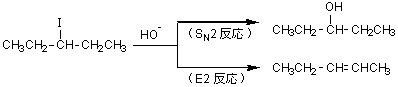 ハロゲン化アルキルと塩基性の強い求核試薬(HO-、RO-など)の反応では、SN2などの求核置換反応とE2などの脱離反応が競争して起こる。SN2反応では脱離基のハロゲンと求核試薬が置換した置換生成物が生じ、E2反応ではハロゲンと隣接炭素の水素がハロゲン化水素(この場合はHI)として脱離して、アルケンを生成する。この問題の場合は、左右どちらの水素が脱離しても生成するアルケンは同じ。
ハロゲン化アルキルと塩基性の強い求核試薬(HO-、RO-など)の反応では、SN2などの求核置換反応とE2などの脱離反応が競争して起こる。SN2反応では脱離基のハロゲンと求核試薬が置換した置換生成物が生じ、E2反応ではハロゲンと隣接炭素の水素がハロゲン化水素(この場合はHI)として脱離して、アルケンを生成する。この問題の場合は、左右どちらの水素が脱離しても生成するアルケンは同じ。
12)
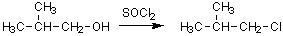 塩化チオニル(SOCl2)はOHをClに変換する試薬として用いられる。したがって、アルコールからはクロロアルカンが生成する。
塩化チオニル(SOCl2)はOHをClに変換する試薬として用いられる。したがって、アルコールからはクロロアルカンが生成する。
13)
 12)と同様に、三臭化リン(PBr3)はOHをBrに変換する。
12)と同様に、三臭化リン(PBr3)はOHをBrに変換する。
14)
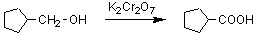 二クロム酸カリウム(K2Cr2O7)は酸化剤。第一級アルコールを酸化するとカルボン酸を生じる。炭素数は変化しないことに注意。CH2OHの炭素がCOOHの炭素になる。
二クロム酸カリウム(K2Cr2O7)は酸化剤。第一級アルコールを酸化するとカルボン酸を生じる。炭素数は変化しないことに注意。CH2OHの炭素がCOOHの炭素になる。
15)
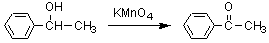 過マンガン酸カリウム(KMnO4)も酸化剤として働く。第二級アルコールは酸化によってケトンに変換される。
過マンガン酸カリウム(KMnO4)も酸化剤として働く。第二級アルコールは酸化によってケトンに変換される。
16)
 カルボニル化合物の求核付加反応の典型的な例。シアン化水素(H-C≡N)から生じたシアン化物イオン(N≡C-)が求核試薬としてプラスに分極したカルボニル炭素を攻撃し、C=O二重結合にシアン化水素が付加したシアノヒドリンが生成する。
カルボニル化合物の求核付加反応の典型的な例。シアン化水素(H-C≡N)から生じたシアン化物イオン(N≡C-)が求核試薬としてプラスに分極したカルボニル炭素を攻撃し、C=O二重結合にシアン化水素が付加したシアノヒドリンが生成する。
17)
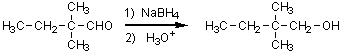 水素化ホウ素ナトリウム(NaBH4)は還元剤として働き、アルデヒドを第一級アルコールに還元する。この反応も炭素数に変化がないことに注意。CHOの炭素はCH2OHの炭素となる。反応機構は、NaBH4から生じたヒドリドイオン(H-)のカルボニル基への求核付加反応。
水素化ホウ素ナトリウム(NaBH4)は還元剤として働き、アルデヒドを第一級アルコールに還元する。この反応も炭素数に変化がないことに注意。CHOの炭素はCH2OHの炭素となる。反応機構は、NaBH4から生じたヒドリドイオン(H-)のカルボニル基への求核付加反応。
18)
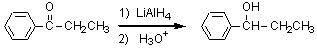 17)と同様に水素化アルミニウムリチウム(LiAlH4)もヒドリドイオンを発生する還元剤。ケトンは還元すると第二級アルコールとなる。
17)と同様に水素化アルミニウムリチウム(LiAlH4)もヒドリドイオンを発生する還元剤。ケトンは還元すると第二級アルコールとなる。
19)
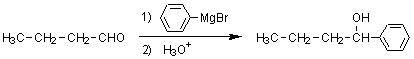 グリニャール試薬(R-MgX)はC-Mg結合の炭素がマイナス、マグネシウムがプラスに分極しており、求核試薬としてカルボニル
基に求核付加を起こす。この問題ではグリニャール試薬のフェニル基が求核試薬としてアルデヒドのC=Oに付加するので、フェニル基が炭素に結合した第二級
アルコールとなる。17)のヒドリド還元と異なり、アルデヒドからは第二級アルコールが生成することに注意。
グリニャール試薬(R-MgX)はC-Mg結合の炭素がマイナス、マグネシウムがプラスに分極しており、求核試薬としてカルボニル
基に求核付加を起こす。この問題ではグリニャール試薬のフェニル基が求核試薬としてアルデヒドのC=Oに付加するので、フェニル基が炭素に結合した第二級
アルコールとなる。17)のヒドリド還元と異なり、アルデヒドからは第二級アルコールが生成することに注意。
20)
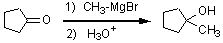 グリニャール試薬とケトンの反応。この場合はメチル基が求核試薬となるので、生成物はメチル基が新たに結合した第三級アルコールとなる。
グリニャール試薬とケトンの反応。この場合はメチル基が求核試薬となるので、生成物はメチル基が新たに結合した第三級アルコールとなる。
21)
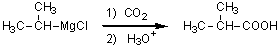 グリニャール試薬とCO2の反応ではカルボン酸を合成できる。CO2もカルボニル化合物と考えられるので、この反応はCO2へのグリニャール試薬の求核付加である。
グリニャール試薬とCO2の反応ではカルボン酸を合成できる。CO2もカルボニル化合物と考えられるので、この反応はCO2へのグリニャール試薬の求核付加である。
22)
 カルボニル基のα炭素から水素が引き抜かれてアニオンとなり、他のカルボニル基に求核付加するのがアルドール反応。この問題では、1分子のプロパナールのα炭素がアニオンとなり、もう1分子のプロパナールのカルボニル基に求核付加する。
カルボニル基のα炭素から水素が引き抜かれてアニオンとなり、他のカルボニル基に求核付加するのがアルドール反応。この問題では、1分子のプロパナールのα炭素がアニオンとなり、もう1分子のプロパナールのカルボニル基に求核付加する。
23)
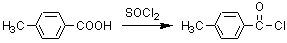 12)でも示したように、塩化チオニル(SOCl2)はOHをClに変換することができるから、カルボン酸のCOOHはCOClに変換されて酸塩化物となる。
12)でも示したように、塩化チオニル(SOCl2)はOHをClに変換することができるから、カルボン酸のCOOHはCOClに変換されて酸塩化物となる。
24)
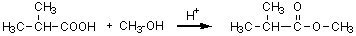 カルボン酸とアルコールを酸触媒を用いて反応させると、脱水反応によってエステルが生成する。
カルボン酸とアルコールを酸触媒を用いて反応させると、脱水反応によってエステルが生成する。
25)
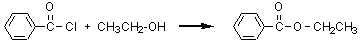 酸塩化物もアルコールと反応してエステルを生成するが、こちらは脱HCl反応である。
酸塩化物もアルコールと反応してエステルを生成するが、こちらは脱HCl反応である。
26)
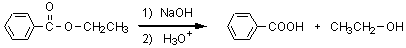 エステルは水酸化ナトリウムのようなアルカリによって加水分解を受け、カルボン酸とアルコールに分解される。
エステルは水酸化ナトリウムのようなアルカリによって加水分解を受け、カルボン酸とアルコールに分解される。